RNA测序、分析+实验验证,探究子痫前期的发病机制
今天和大家分享一篇发表在Mol Ther Nucleic Acids.有关RNA测序、分析+实验验证的文章。题目为:Preeclampsia-Associated lncRNA INHBA-AS1 Regulates the Proliferation, Invasion, and Migration of Placental Trophoblast Cells。
研究背景:
子痫前期(preeclampsia, PE)是妊娠期特有的综合征,主要表现为妊娠20周后新发高血压和蛋白尿,可伴有其他系统疾病表现。目前子痫前期的病因和发病机制尚不明确,有研究认为其可能的机制包括:血管内皮受损、 炎症免疫过度激活、营养缺乏、遗传因素、胰岛素抵抗等,发病主要可能与滋养细胞浸润不足导致子宫螺旋动脉重铸障碍有关。长链非编码RNA(long noncoding RNA, lncRNA)是指转录本长度超过200核苷酸数(nucleotide,nt) 的RNA分子。已有研究发现lncRNA在子痫前期患者胎盘中相对正常对照组出现异常表达,并影响滋养细胞增殖、迁移、侵袭、凋亡等功能。如 IGF2 /H19 MEG3, SPRY4-IT1,HOTAIR, MALAT1, FLT1P1 CEACAMP8 可以通过甲基化、 Notch-EGFL7 信号通路、Wnt /β-catenin 信号通路等方式导致子痫前期。LncRNA-mRNA 共表达分析发现其在脂质代谢和 2 型免疫应答等通路中均有显著参与, 这与子痫前期相对正常妊娠其代谢和免疫状态受到影响的理论一致。
研究方法:作者所在的研究团队收集了2015年5月-2016年1月南方医院产科剖宫产分娩的9例重症早发子痫前期(early-onset severe preeclampsia, EOSPE)及32例正常对照组胎盘组织样本进行RNA测序,通过测序结果发现在重症早发子痫前期患者胎盘中相对正常对照组高表达的lncRNA INHBA-AS1(INHBA antisense RNA 1)。进一步收集2016年5月-2017年1月南方医院产科剖宫产分娩的27例子痫前期和31例正常对照组胎盘样本进行实时荧光定量PCR(quantitative real-time PCR, qRT-PCR)验证,同样显示lncRNA INHBA-AS1在子痫前期中表达显著上调。接着在滋养细胞系HTR-8/SVneo中研究lncRNA INHBA-AS1的生物学功能和可能的作用机制;同时用CRISPR/Cas9技术敲除lncRNA INHBA-AS1后,进一步研究其功能;通过荧光原位杂交(Fluorescent In Situ Hybridization, FISH)和核质分离实验定位lncRNA INHBA-AS1。接下来通过RNA pull down实验对lncRNA INHBA-AS1结合的蛋白进行质谱分析, 对结合蛋白进行GO-CC分析;通过生信分析寻找受lncRNA INHBA-AS1调控的转录因子及转录因子的靶基因,通过RIP实验反向验证了lncRNA INHBAAS1与分析结果中的转录因子结合。进一步利用CHIP和荧光素酶报告基因实验证明lncRNA INHBAAS1结合相应的转录因子从而影响靶基因的转录。同时,靶基因可以影响侵袭/迁移相关通路蛋白MMP2、 MMP3、 Vimentin。
研究结果:
1. LncRNA INHBA-AS1 在 EOSPE 胎盘中高表达
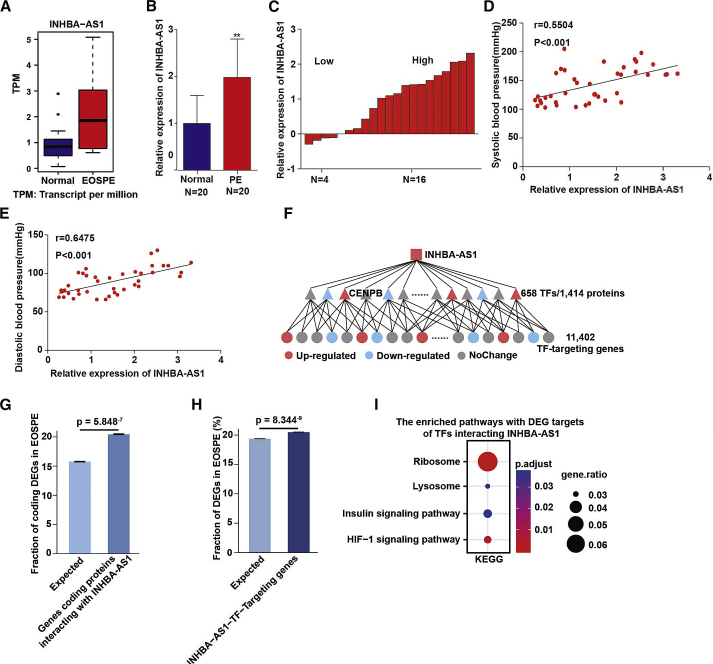
在作者的前期研究中,采集了9例EOSPE胎盘样本和32例正常对照组胎盘样本,进行RNA测序,测序结果显示lncRNA INHBA-AS1 在 EOSPE胎盘样本中相对正常对照组表达量升高,实时荧光定量PCR实验结果发现85%(23/27)的子痫前期患者胎盘lncRNA INHBA-AS1 明显上调。并且发现孕妇收缩压与 lncRNA INHBA-AS1 的表达量呈正相关。 孕妇舒张压与 lncRNA INHBAAS1 表达量的相关性结果同样呈正相关。提示 lncRNA INHBA-AS1 与患者的一些临床数据关系密切。为了确定 INHBA-AS1-蛋白质复合物的功能性细胞
定位,进行 Gene Ontology (GO)富集分析, 发现 lncRNA INHBA-AS1 结合蛋白可能与细胞核中的复合物相关。
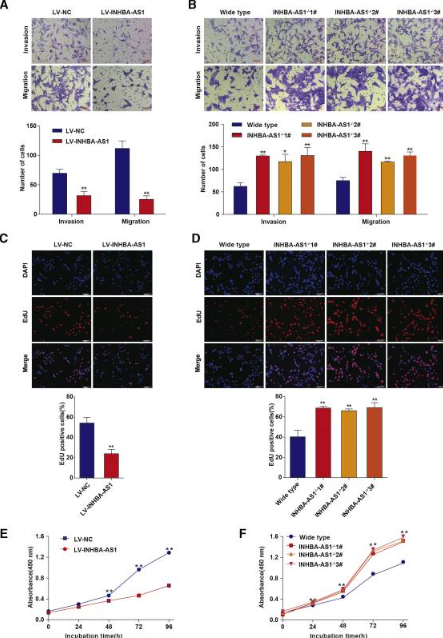
2. LncRNA INHBA-AS1影响滋养细胞生物学功能
作者通过在HTR-8/SVneo 细胞中过表达和敲除LncRNA INHBA-AS1,对功能进行探索发现:过表达lncRNA INHBA-AS1抑制HTR-8/SVneo 细胞的侵袭/迁移、增殖能力;促进了凋亡能力。删除 lncRNA INHBA-AS1 促进HTR-8/SVneo细胞的侵袭/迁移、增殖能力,抑制了凋亡能力。
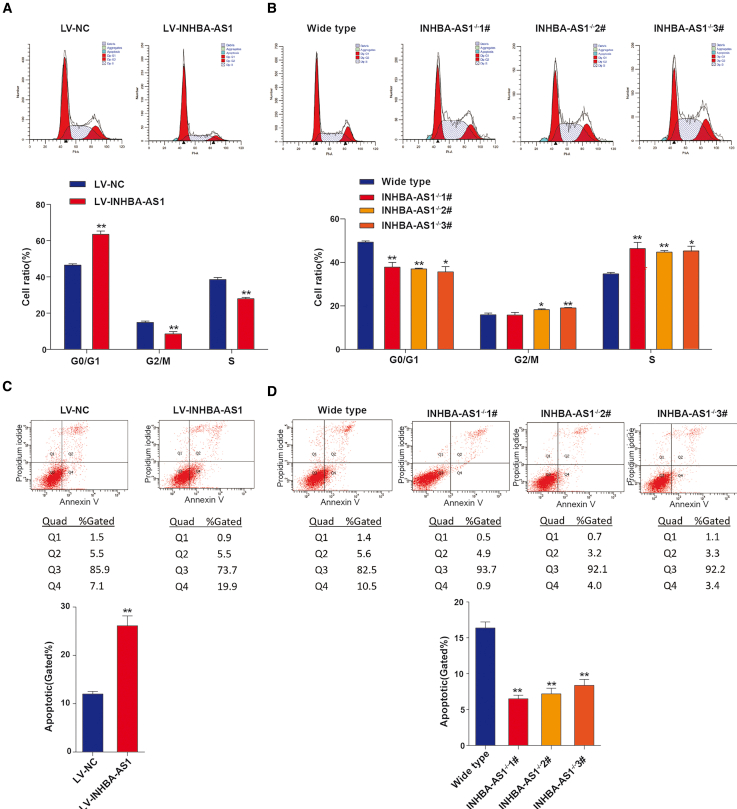
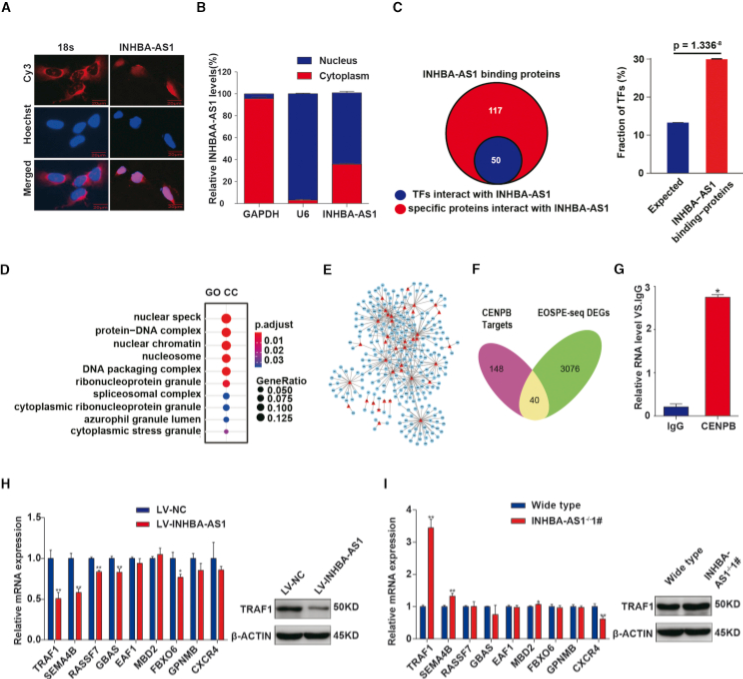
3.INHBA-AS1 结合 CENPB 调控 INHBA 和 TRAF1
作者利用FISH和细胞核质分离实验对INHBA-AS1的定位进行了探究,发现 lncRNA INHBA-AS1主要在细胞核中表达,说明lncRNA INHBA-AS1可能参与转录调控过程。为了寻找与 lncRNA INHBA-AS1 结合的蛋白质,进行了RNA-pulldown实验和质谱检测,检测到lncRNA INHBA-AS1 蛋白复合物中的 167 个蛋白,其中有45个转录因子显示出显著的富集。为了确定 INHBA-AS1-蛋白质复合物的功能性细胞定位,进行 Gene Ontology (GO)富集分析,发现 lncRNA INHBA-AS1 结合蛋白可能与细胞核中的复合物相关,进一步验证了 lncRNA INHBAAS1 位于细胞核中并参与转录或其相关过程。同时作者通过生信分析方法,构建了转录因子-靶基因调控网络,在网络中发现CENPB具有第二高的中介中心性。说明CENPB可能在该调控网络中发挥重要作用。为了进一步验证 lncRNA INHBA-AS1 与转录因子 CENPB 结合,作者通过 RNA 免疫沉淀(RIP)实验进行了反向验证,得出了一致的结论。
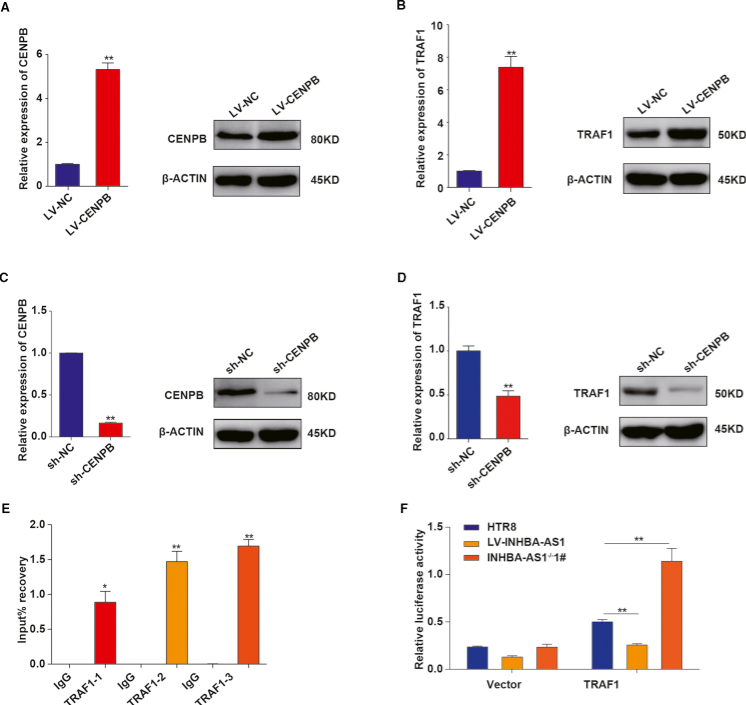
4.CENPB 通过结合 INHBA 和 TRAF1 的启动子区促进其转录
为了研究转录因子CENPB对INHBA和TRAF1的影响,作者建立HTR-8/SVneo细胞的CENPB过表达稳定细胞株,通过qRT-PCR发现INHBA 和 TRAF1 的 mRNA 和蛋白水平均较对照组升高,相反, 当 HTR-8/SVneo 细胞中 CENPB 被敲除时,INHBA 和 TRAF1 的 mRNA 水平和蛋白水平较对照组下降。同时染色质免疫沉淀(ChIP)实验检证实 CENPB 与 INHBA 和 TRAF1 启动子区域相结合。 接下来,通过荧光素酶报告基因实验分别检测 HTR-8/SVneo细胞系、INHBA-AS1过表达细胞系、INHBA- AS1敲除细胞系中,INHBA启动子区域片段(INHBA-2)和TRAF1启动子区域片段(TRAF1-3)启动子活性的改变。荧光素酶报告基因实验结果显示 lncRNA INHBA- AS1 抑制 CENPB 对INHBA 和 TRAF1 启动子的促转录作用。
5. INHBA-AS1通过INHBA和TRAF1对HTR-8/SVneo细胞侵袭/迁移发挥作用
作者通过前期的生信分析和实验证明lncRNA INHBA-AS1通过结合CENPB抑制胎盘滋养层细胞的侵袭和迁移,且CENPB可以结合INHBA和TRAF1 的启动子区调控其转录。为了进一步确认 lncRNA INHBA-AS1 在 HTR-8 / SVneo 细胞中通过结合 CENPB调节INHBA 和TRAF1 的转录,作者在 HTR-8 / SVneo 细胞中分别过表达 lncRNAINHBA-AS1, INHBA, TRAF1以及在过表达 INHBA-AS1 的 HTR-8 /Svneo 稳定细胞株中转染空载 pcDNA3.1, pcDNA3.1-INHBA, pcDNA3.1-TRAF1。结果提示,过表达INHBA-AS1可以抑制滋养细胞的侵袭和迁移,而INHBA或TRAF1 可部分恢复 HTR-8/SVneo 细胞被 INHBA- AS1 所阻断的侵袭和迁移功能,接下来也检测到了MMP2、MMP3和Vimentin 这几个参与细胞侵袭和迁移通路的关键分子在 HTR-8 / SVneo 细胞过表达 INHBA 和 TRAF1后出现上调。在敲除 INHBA-AS1的HTR-8 / Svneo稳定细胞株中分别转染 si-NC,si-INHBA,si- TRAF1。Transwell 结果显示敲除INHBA-AS1 促进了 HTR-8/SVneo 细胞的侵袭和迁移,进一步敲低 INHBA 或TRAF1 可部分抑制 INHBA-AS1 对 HTR-8/SVneo 细胞侵袭和迁移能力的促进作用。与此同时,敲低 INHBA 或 TRAF1 后,MMP2、MMP3、Vimentin等侵袭迁移标志物表达下调。
总结:
作者通过对EOSPE患者胎盘进行RNA测序,生信分析结果提示,lncRNA INHBA-AS1的表达量存在显著差异。通过扩大样本收集子痫前期患者胎盘与正常产妇胎盘,进一步验证了 lncRNA INHBA-AS1在子痫前期患者胎盘中表达量升高,且发现表达水平与孕妇血压呈正相关。进一步探究 lncRNA INHBA-AS1的上调如何参与子痫前期的发病。通过生信分析及实验发现lncRNA INHBA- AS1与转录因子CENPB结合,从而抑制下游靶基因INHBA、TRAF1的转录, 影响滋养细胞的侵袭和迁移,从而参与子痫前期的发病机制。
拓普生物目前向广大医务工作者提供"科研随航服务”,该服务团队为临床PI和一线科研工作者组成,为您量身打造整套的科研规划,让您快乐科研,轻松工作,为您的科研之路和晋升之路保驾护航,详情请咨询:0755-86325431 或点击下方微信扫码咨询:






